中学入試・高校入試の化学分野を紹介します。今回は「電気分解」を解説します。
もくじ
電気分解とは?
電気分解とは化合物に電気を加えて化学分解することです。
原理的には酸化還元反応が起こることです。化合物を電気で分解することです。
基本的な電気分解の仕組み
電気を使って化合物を分解することが電気分解と言いました。従って電気分解ができる化合物は電気が通らなくてはなりません。具体的には電解質の溶液に電極を差し込み、電気を流して電解質を分離させます。
電気分解で比較的安定している化合物を分離することができます。
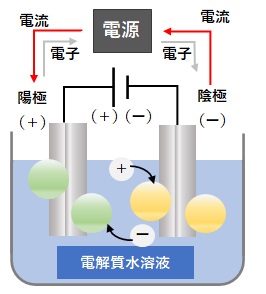
電気分解の原理の図
電解質と非電解質
電解質は電気を通す物質のことです。非電解質は電気を通さない物質です。
電解質の主な例
食塩・水酸化ナトリウム・塩化銅・硫酸など
非電解質の主な例
アルコール・砂糖・ゴムなど
電気分解では電解質を使います。


電気分解の例
水の電気分解
白金(プラチナ)を電極として水に電流を流します。すると水は電気分解を起こします。陰極(-極)に水素(H2)が発生し、陽極(+極)に酸素(O2)が発生します。
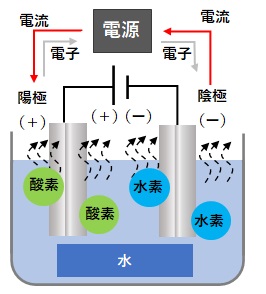
水の電気分解の図
塩酸の電気分解
白金(プラチナ)、炭素棒などを電極として水に電流を流します。すると水は電気分解を起こします。陰極(-極)に水素(H2)が発生し、陽極(+極)に塩素(Cl2)が発生します。
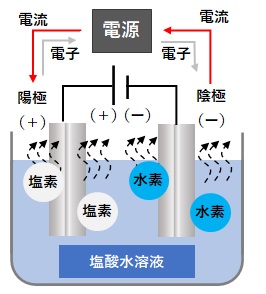
塩酸の電気分解の図
塩化銅の電気分解
炭素棒を電極として塩化銅水溶液に電流を流します。すると塩化銅水溶液は電気分解を起こします。陰極(-極)に銅(Cu)が発生し、陽極(+極)に塩素(Cl2)が発生します。
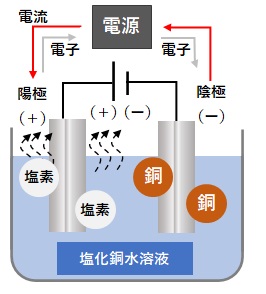
塩化銅水溶液の電気分解の図
電気分解と電池
電気分解は酸化還元反応を起こすことです。この酸化還元反応を利用して電流を流す仕組みのことを電池といいます。
電池は充電できないものと充電できるものがあります。
充電できないもの
マンガン乾電池…懐中電灯、リモコンで使用される
リチウム電池…電卓・カメラで使用される
ボルタ電池…1800年イタリアのボルタによって考案された
ダニエル電池…1836年イギリスのダニエルによって考案された
充電できるもの
鉛蓄電池…自動車のバッテリー
ニッケルカドミウム電池…コードレス機器
リチウム電池…携帯電話、ノートパソコン、電気自動車



電気分解とファラデーの法則(補足)
中学入試と高校入試では出ませんが、ファラデーの法則というものがあります。水溶液の電気分解において、陰極または陽極で変化される物質の量は、流した電気量に比例するというものがあります。
これをファラデーの法則と言います。
中学受験コースはこちら
高校受験コースはこちら







-440x290.jpg)


